Función ácido
Ácidos hidrácidos
Son combinaciones binarias de hidrógeno con los halógenos (F, Cl, Br, I) y los calcógenos (S,
Se y Te).
Hidrógeno + No metal ----->Ácido hidrácido
Formulación: Para formular los hidrácidos escribimos el hidrógeno seguido del no metal y
después se intercambian las valencias.
El hidrógeno actúa con número de oxidación +1; F, Cl, Br e I actúan con número de oxidación
-1, y S, Se y Te con -2.
Estos compuestos, al disolverse en agua, dan origen a ácidos (hidrácidos).
Nomenclatura
• Tradicional: Se nombran con la palabra ácido seguida de la raíz del no metal y la terminación
- hídrico.

Oxoácidos
Las combinaciones binarias del hidrógeno con halógenos y calcógenos son ácidos (excepto
el agua, H2O). Otros compuestos con propiedades ácidas, caracterizados por contener
oxígeno en la molécula, son los oxoácidos. Estos responden a la siguiente fórmula general:
H = hidrógeno con número de oxidación +1
HaXbOc X = elemento no metálico o metálico, con
número de oxidación positivo
O = oxígeno con número de oxidación −2
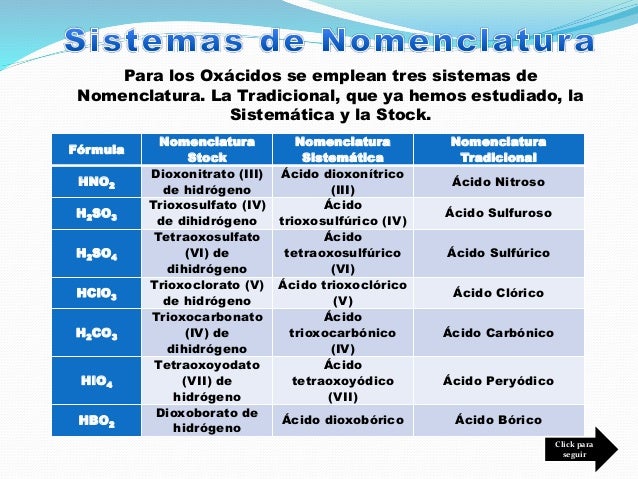
Se clasifican y se nombran según el número de oxidación del átomo central. En los oxoácidos
más comunes, el átomo central es un no metal con subíndice 1.
Si el elemento central del oxoácido es un metal, se trata de un metal de transición con un
número de oxidación elevado. Por ejemplo:
• H2MnO4, ácido mangánico • HMnO4, ácido permangánico
• H2ReO4, ácido rénico • HReO4, ácido perrénico
• H2CrO4, ácido crómico • H2Cr2O7, ácido dicrómico
Para nombrarlos utilizamos principalmente la nomenclatura clásica, aceptada por la IUPAC.
Los nombramos con la palabra ácido seguida del nombre del elemento central acompañado
de prefijos y sufijos en función de su número de estados de oxidación.
Reglas para ayudar a formular oxoácidos
Debemos tener en cuenta que los sufijos -oso e -ico y los prefijos hipo- y per- nos informan
del número de oxidación del elemento central.
Los prefijos meta- y orto- indican la existencia de menos o más hidrógenos y oxígenos.
El prefijo di- se utiliza cuando el número de átomos del elemento central es el doble de
lo esperado.
En los ácidos que no utilizan el prefijo di- se cumple que:
• Si el número de oxidación del elemento central es impar, el número de hidrógenos
en la fórmula será impar.
• Si el número de oxidación del elemento central es par, el número de hidrógenos en
la fórmula tiene que ser par.
Función de los ácidos
Los hidrácidos, en la actualidad, tienen gran importancia en la industria química, ya que están presentes en casi todos los elementos que se utilizan para elaborar los productos de
aseo personal. Por ejemplo en los jabones juegan un papel fundamental, aunque claro las concentraciones no son elevadas, pues, caso contrario, sería dañino para la piel.

Los hidrácidos también están presentes en los champús, en las pastas dentales, en los
acondicionadores para cabello, en los cosméticos. Los hidrácidos resultan imprescindibles
en muchos productos de aseo personal, belleza y maquillaje, de ahí su gran importancia para el desarrollo de las industrias. También son usados en algunos alimentos.
Los ácidos oxoácidos también tienen un gran uso industrial como el ácido nítrico que
sirve para fabricar abonos, colorantes, plásticos, explosivos, medicamentos y grabado de metales.
El ácido carbónico se usa en jardinería, gaseosas, helados y alimentos congelados.
El ácido sulfúrico se utiliza en la fabricación de fertilizantes, detergentes, papel, refinación
de petróleo y procesamiento de metales.
No hay comentarios:
Publicar un comentario